Акушерство для студентів І та ІІ рівнів акредитації
Головне меню
Аномалії розвитку та захворювання елементів заплідненої яйцеклітини
Актуальність теми
За сучасних умов особливого значення набуває пренатальна діагностика вад розвитку плода, оскільки стан екології вкрай несприятливо позначається на спадковості популяції. Слід розрізняти поняття вродженої та спадкової патології. Причиною спадкових захворювань є патологічна спадковість, одержана організмом дитини через статеві клітини її батьків (хромосомні хвороби); випадки успадкування простежуються в родоводі. Причинами вроджених захворювань можуть бути чинники зовнішнього середовища, що впливають на плід у критичні періоди розвитку.
Акушерка повинна пам’ятати про критичні періоди розвитку та негативний вплив шкідливих чинників, і не лише оточуючого середовища, а й лікарських засобів та перинатальних інфекцій.
Знати:
1. Вплив шкідливих чинників на розвиток плода.
2. Критичні періоди вагітності.
3. Аномалії плаценти, водної оболонки та пуповини: клініку, методи діагностики.
4. Особливості перебігу вагітності при даній патології.
5. Особливості ведення вагітності та пологів у жінок із аномаліями розвитку та захворюваннями елементів заплідненого яйця.
Вміти:
-
-
-
Виконувати навички:
-
-
-
-
Література:
Акушерство та гінекологія: У 4 т.: національний підручник / за ред. акад. НАМН України, проф. В.М. Запорожана. — К.: ВСВ “Медицина”, 2013. — С. 97-
Запорожан В. М., Цегельський М. Р., Рожковська Н. М. Акушерство і гінекологія. Підручник: У 2-
Наказ МОЗ України № 417 від15.07.2011. Про організацію амбулаторної акушерсько-
Наказ МОЗ України № 641/84 від 31.12.2003. Про удосконалення медико-
Режим доступу: http://www.moz.gov.ua/ua/print/dn_20031231_641_.html
Патологічне і оперативне акушерство: підручник / І.Б. Назарова, В.Б. Самойленко, Н.П. Муштенко, І.Г. Шембєлєв; за ред. П.М. Баскакова. — К.: ВСВ «Медицина», 2012. — С. 143-
Запитання для самоконтролю до теми «Аномалії розвитку та захворювання елементів заплідненої яйцеклітини»
1. Дайте визначення термінам бласто-
2. Назвіть критичні періоди вагітності, шкідливі чинники, їх вплив на зародок та плід.
3. Назвіть аномалії пуповини, їх вплив на плід.
4. Опишіть аномалії амніона (маловоддя, багатоводдя), особливості перебігу вагітності, особливості ведення пологів.
5. Опишіть аномалії трофобласта (міхурцевий занесок), діагностика, ускладнення, тактика, лікування, диспансеризація.
6. Опишіть аномалії плаценти, особливості перебігу вагітності, особливості ведення пологів при цій патології.
7. Назвіть причини внутрішньоутробної загибелі плода.
8. Опишіть методи діагностики внутрішньоутробної загибелі плода.
9. Опишіть акушерську тактику при внутрішньоутробній загибелі плода.
10. Назвіть принципи медико-
11. Назвіть методи діагностики фетоплацентарної недостатності.
12. Опишіть роль акушерки в перинатальній охороні плода.
Аномалії розвитку та захворювання елементів заплідненої яйцеклітини
Більшість аномалій виявляються при народженні дитини (у 2–3 % новонароджених), ще 2–3 % аномалій виявляють протягом перших 5 років життя, що загалом становить 4–6 %.
Вроджені аномалії є основною причиною дитячої смертності (21 % від усіх причин). Вони є основною причиною непрацездатності і займають п’яте місце серед причин вкорочення потенційного життя до 65 років.
Причини природжених вад у 40–60 % випадків залишаються нез’ясованими. Генетичні чинники (хромосомні аномалії і мутантні гени) зумовлюють близько 15 % вад, агресивні фактори зовнішнього середовища спричинюють близько 10 % природжених вад, а комбінації генетичних чинників з факторами зовнішнього середовища (мультифакторіальна спадковість) — 20–25 %. Багатоплідна вагітність спричинює 0,5–1 % аномалій розвитку. Більшість природжених вад розвитку виникає в період органогенезу — між 3 і 8-
Багато випадків природжених вад можна попередити. Так, вживання йодованої солі запобігає розвитку кретинізму, що проявляється розумовою відсталістю і деформаціями кісток. Суворий метаболічний контроль за пацієнтками з цукровим діабетом і фенілкетонурією дозволяє зменшити ризик природжених вад розвитку. Додавання у харчовий раціон фолатів до запліднення і протягом вагітності зменшує ризик розвитку дефектів нервової трубки (щілина хребта, аненцефалія).
Критичні періоди розвитку ембріона і плода
1) перший період, преембріональний, який триває після запліднення протягом першого тижня вагітності. Критичними моментами цього періоду є запліднення і імплантація. Дія несприятливих факторів у цей період спричинює ембріотоксичний ефект або відсутність будь-
2) другий період — ембріональний, триває з 3 до 8-
3) третій, фетальний (плодовий) період, триває з 9-
ВАДИ РОЗВИТКУ ПЛОДА
Залежно від часу та об'єкта ураження виділяють:
-
-
-
Гаметопатії
Гаметопатії — захворювання, пов'язані з ушкодженням або аномаліями статевих клітин.
Причини: спорадичні мутації статевих клітин батьків
або
успадкуванння від віддалених поколінь.
Успадковуються за домінантним або рецесивним типом,
ризик з домінантним типом успадкування – 50%.
ризик захворювання якщо батьки носії однакового рецесивного гена – 25%.
Найчастішими спадковими захворюваннями є муковісцидоз, фенілкетонурія, адреногенітальний синдром, хвороба Дауна тощо.
Хромосомні аномалії
Хромосомні аномалії включають кількісні аномалії або структурні аномалії і є важливим фактором мимовільних викиднів і вроджених аномалій розвитку.
50 % усіх запліднень завершуються мимовільними викиднями і в 50 % випадків цих викиднів наявні хромосомні аномалії.
Найбільш частими хромосомними аномаліями в абортусів є 45,Х (синдром Тернера, або Шерешевського — Тернера), триплоїдія і трисомія 16. Хромосомні аномалії є причиною 7 % великих природжених вад розвитку, а мутації генів — близько 8 %.
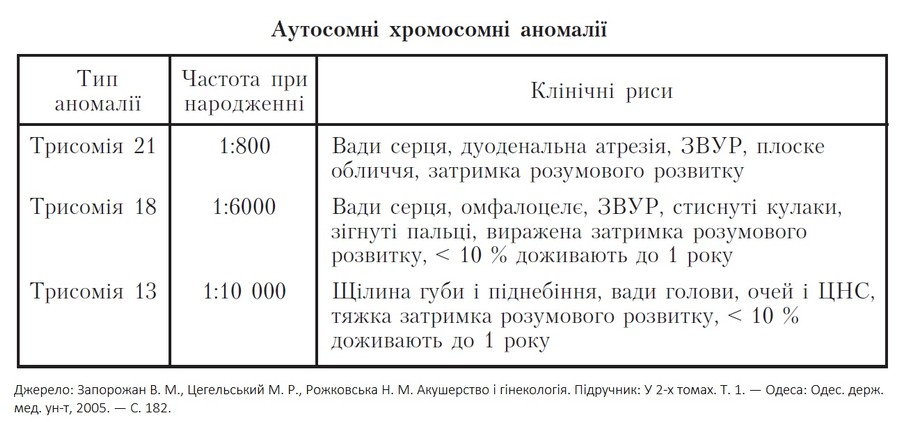
Кількісні аномалії хромосом
Трисомія 21 (синдром Дауна) найчастіше зумовлена наявністю зайвої копії хромосоми 21 (трисомія 21). Дітям із синдромом Дауна притаманні: затримка росту, різні ступені розумового відставання, черепнолицеві аномалії (епікант, скошений розріз очей, плоске обличчя, маленькі низько розміщені вуха), вади розвитку серця,
гіпотонія та ін. У таких дітей частіше мають місце інфекції, дисфункції щитоподібної залози, передчасне старіння, розвиток хвороби Альцгеймера у молодому віці (з 35 років). У 95 % випадків синдром зумовлений трисомією 21 через мейотичне нерозходження, у 75 % випадків нерозходження трапляється під час оогенезу. Частота синдрому Дауна становить 1:2000 запліднень у жінок віком < 25 років і зростає до 1:300 — у віці 35 років і 1:100 — у віці 40 років.
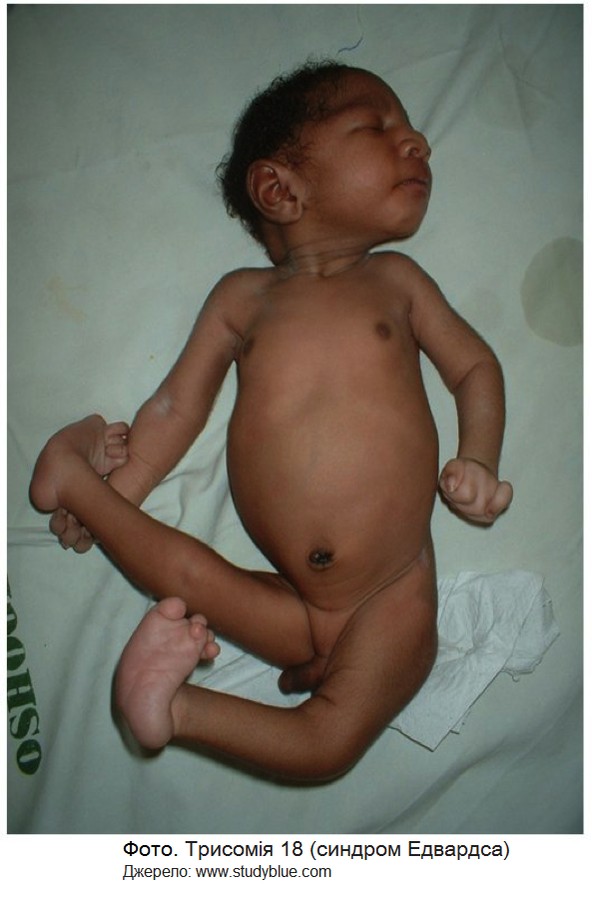
Трисомія 18 (синдром Едвардса) зустрічається з частотою 1:5000 новонароджених і характеризується розумовою відсталістю, мікрогнатією, природженими вадами серця, нирок, скелета, зігнутими пальцями та синдактилією. Такі діти звичайно вмирають у віці до 2 міс.
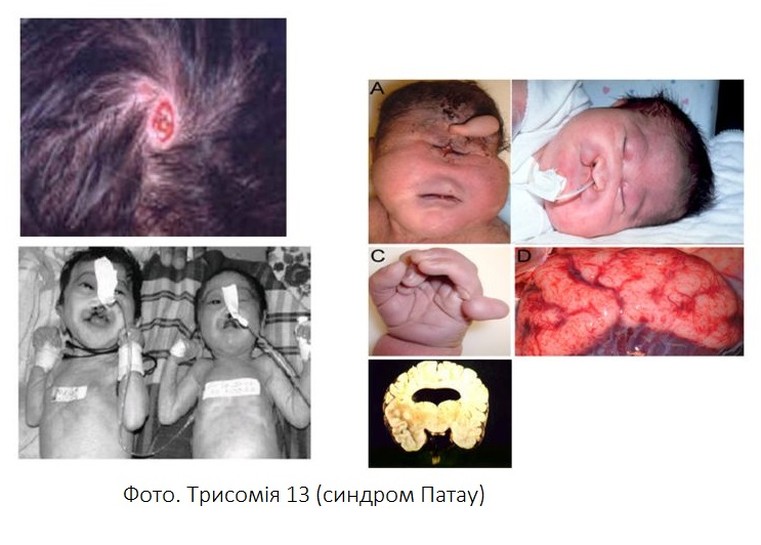
Трисомія 13 (синдром Патау) є рідкісним захворюванням (1:15 500 живих новонароджених) і включає розумову відсталість, природжені вади серця, глухоту, розщілини губи і піднебіння, очні вади (мікрофтальмія, анофтальмія). Більшість дітей вмирають у віці до 3 міс.
Синдром Кляйнфельтера (XXY або XXXY) проявляється в осіб чоловічої статі в період статевого дозрівання і характеризується атрофією яєчок, безплідністю і, часто, гінекомастією. Частота 1:500 чоловіків. Клітини містять 47 хромосом з додатковою Х хромосомою (генотип ХХY). Синдром звичайно не супроводжується затримкою розумового розвитку.
Синдром Тернера, Шерешевського — Тернера (ХО, структурні аномалії або мозаїцизм). Синдром характеризується жіночим генотипом за відсутності яєчників (дисгенезія гонад, або гонадний дисгенез). Хворі мають низький зріст, широку грудну клітку з великою відстанню між сосками, деформації скелета, перетинчасту шию.
Синдром трисомії Х (ХХХ) характеризується певним ступенем розумової відсталості, затримкою статевого розвитку, гіпоменореєю. В клітинах містяться по 2 тільця статевого хроматину.
Структурні аномалії хромосом
Ці аномалії можуть стосуватися однієї або більше хромосом і зазвичай виникають через розриви хромосом.
Розриви можуть бути спричинені дією агресивних факторів зовнішнього середовища: вірусів, радіації або хімічних речовин.
Наприклад, синдром «котячого крику» зумовлений частковою делецією короткого плеча хромосоми 5 і характеризується мікроцефалією, розумовою відсталістю, природженими вадами серця. Плач таких дітей нагадує котячий крик.
Генні мутації
Моногенні генетичні захворювання: серповидноклітинна анемія, муковісцидоз, фенілкетонурія, галактоземія.
Полігенні генетичні захворювання: хвороба Альцгеймера, діабет, ожиріння, артрит.
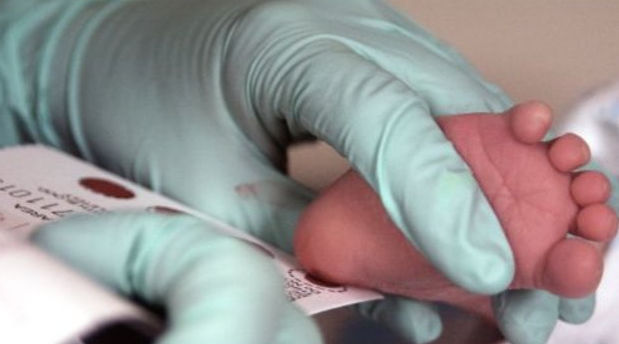
Фото. Скринінгове обстеження на фенілкетонурію (ФКУ) проводиться всім новонародженим до виписки (на 3-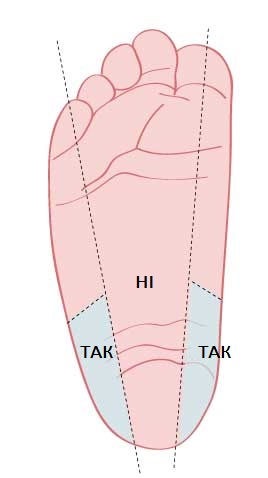
Мал. Вказано місце пунктування на п’яточці новонародженого для взяття крові на ФКУ
(медіально від лінії, проведеної від великого пальця до п'яти чи латерально від лінії, проведеної від проміжку між 4-

Ембріопатії
Ембріопатії — захворювання, що виникають у перші 3 місяці вагітності в процесі органогенезу.
Вплив тератогених факторів у період диференціювання органів може призвести до виникнення вад розвитку.
Органи вражаються у послідовності: очі, мозок, серце, органи слуху, кістки.
Наприклад, дія шкідливих чинників на 4-
Тератогенні фактори. Дивись таблицю "Вплив тератогенів на розвиток людини"
вірусні захворювання матері
краснуха,
вітряна віспа,
кір, грип,
фізичні фактори
рентгенівське випромінювання,
ультрафіолетове випромінювання,
іонізуюче випромінювання,
хімічні фактори
ртуть,
алкоголь,
нікотин,
деякі лікарські препарати
недостатнє та неповноцінне харчування матері,
ендокринна патологія (цукровий діабет).
Фетопатії
Фетопатії — внутрішньоутробне ураження уже сформованих органів та систем плода.
У II і III триместрах вагітності відбувається дозрівання функціональних систем плода, становлення функцій, необхідних для виживання дитини у позаутробному середовищі.
Вагому роль у виникненні фетопатій має плацента. Бар'єрна функція плаценти є недосконалою щодо багатьох речовин, які потрапляють в організм матері.
Залежно від інтенсивності та тривалості дії шкідливих чинників відбувається затримка розвитку систем плода того чи іншого ступеня.
Наприклад:
-
-
Профілактика, скриніг та діагностика вродженої патології
Джерело: Ефективний антенатальний догляд, навчальний посібник. Швейцарський інститут охорони здоров’я та тропічної медицини. -
Скринінг (від англ. screening «просіювання») -
У медицині під скринінгом мають на увазі проведення простих, безпечних, низьковартісних досліджень, які охоплюють великі групи населення з метою виявлення тієї чи іншої патології.
В Україні скринінгові програми вагітних затверджені наказами МОЗ України :
• скринінг на вроджені вади розвитку плода: структурні аномалії, хромосомну патологію;
• скринінг на інфекції: безсимптомна бактеріурія, вірусний гепатиту В, сифіліс, ВІЛ;
• скринінг на гематологічні проблеми (гемоглобінопатії, тромбоцитопенії),
• визначення групи крові, резус-
• скринінг на клінічні стани (захворювання): гестаційний діабет, прееклампсія.
Пренатальний скринінг (ПС) -
1.Перше скринінгове обстеження проводиться у терміні 11тиж. +1 день -
• УЗД для визначення хромосомної патології (товщина комірцевого простору, наявність/відсутність кісток носу, лицевий кут, трикуспідальна регургітація, кровоплин у венозній протоці), а також терміну вагітності, ознак життєдіяльності плода, кількості плодів тощо.
• Біохімічні маркери -
Вагітним жінкам, чий ризик перевищує граничний, призначається інвазивне обстеження.
Жінкам віком 42 роки і більше у зв’язку з високим віковим ризиком доцільно призначати інвазивні обстеження без проведення скринінгових тестів.
Ефективність скринінгового обстеження 1 триместру для виявлення хромосомної патології складає близько 95%.
2.Друге скринінгове дослідження проводиться у 2 триместрі в терміні 18-
• УЗД для діагностики аномалій плода і ускладнень у перебігу вагітності. Поряд з детальною оцінкою анатомії плода проводиться визначення ехо-
• біохімічний скринінг 2 триместру, для якого існують наступні алгоритми:
а) вагітні із низьким ризиком по хромосомній патології можуть обстежуватися тільки на альфа-
б) вагітні, які не проходили обстеження у 1 триместрі і вперше звернулися тільки у 2 триместрі (до 20 тижнів 6 днів), проводиться:
• АФП+ вільний в-
або
• АФП + вільний в-
У разі виявлення за результатами скринінгу маркерів вроджених вад розвитку плода, високого генетичного ризику хромосомної або іншої вродженої патології, комплексу УЗД ознак, вагітна направляється на консультацію для уточнення діагнозу, визначення прогнозу та вибору тактики ведення вагітності і пологів.
У випадках пренатально виявленої вродженої та спадкової патології проводиться пренатальний консиліум.
ПОКАЗАННЯ ДО НАПРАВЛЕННЯ ВАГІТНОЇ НА МЕДИКО-
1. Вік вагітної 35 років і більше. Вік чоловіка 40 років і більше.
2. Наявність у одного з подружжя спадкової патології, хромосомної перебудови або вродженої(их) вади розвитку.
3. Наявність у вагітної фенілкетонурії, муковісцидозу та інших спадкових захворювань
4. Наявність в родині живих або померлих дітей зі:
-
-
-
-
5. Наявність вищезазначеної патології серед родичів.
6. Кровноспоріднений шлюб.
7. Звичне невиношування вагітності невстановленого генезу у І триместрі вагітності.
8. Несприятливі впливи у ранні терміни вагітності (захворювання, діагностичні або лікувальні процедури, прийом медикаментів).
9. Ускладнений перебіг вагітності (загроза переривання з раннього терміну, яка не піддається терапії, багатоводдя і маловоддя).
10. Вагітні після ДРТ.
11. Патологія плода, виявлена при пренатальному скринінгу (УЗ, біохімічні маркери, високий індивідуальний генетичний ризик виникнення хромосомної та деякої вродженої патології).
12. Наявність у подружжя шкідливих факторів, пов'язаних із професією.
Медико-
ПРЕКОНЦЕПЦІЙНА ПІДГОТОВКА ВАГІТНОЇ ДО НАРОДЖЕННЯ ДИТИНИ Наказ № 417. Додаток 19.
1. Харчування
• Повноцінне харчування під час вагітності. Калорійність раціону має складати близько 2400 ккал/добу. В раціон необхідно включати близько 60-
• Обмежити вживання жирів та вуглеводів.
• Рекомендується щоденно вживати овочі, фрукти, фруктові соки.
• При ожирінні рекомендується білково-
2. Відпочинок та фізичне навантаження
• Не допускати фізичного навантаження, яке пов’язане із підніманням важких предметів, тривалого знаходження у вертикальному положені.
• Уникати перевтоми, нічної праці, тривалого перегляду телевізійних передач. Забезпечувати повноцінний сон у нічний час при відсутності світла (особливо близько 2-
• За умови відсутності акушерських ускладнень рекомендуються фізичні вправи середньої сили з рівномірним навантаженням різних груп м’язів, спеціальні курси аеробіки.
3. Максимально уникати контакту з шкідливими впливами (хімічними, фізичними) як на роботі, так і в побуті.
• Відмова від паління та «пасивного» куріння, вживання алкоголю.
3. Вітамінні та інші біологічно активні комплекси
• Фолієва кислота
Фолієва кислота надходить в організм з продуктами харчування. Найбільша кількість її міститься у фруктах, овочах, шпинаті, спаржі, салаті брокколі, динях, бананах.
При дефіциті фолієвої кислоти розвивається фолієводефіцитна анемія та вади розвитку центральної нервової системи плода.
Рекомендується щоденний прийом 400 мкг фолієвої кислоти до настання вагітності та в ранні строки (до 12 тижнів) для профілактики вад розвитку центральної нервової системи плода.
Якщо в анамнезі відмічались випадки народження плодів/ дітей з вродженими дефектами нервової трубки добова доза фолієвої кислоти складає 800 мкг.
• Полівітаміни та мінерали (поєднання вітаміну А, рибофлавіну, цинку, магнію, кальцію, йоду) – перед заплідненням та в ранні строки вагітності попереджує виникнення вад розвитку у плода та поліпшує стан матері.
4. Оздоровлення жінки:
Лікування вогнищ хронічної інфекції та запобігання гострих інфекційних захворювань
Лікування хронічних захворювань до компенсованого стану.
5. Контроль овуляції та синхронізація процесів овуляції та запліднення
ПАТОЛОГІЯ ПЛОДОВИХ ОБОЛОНОК
Патологія водної оболонки
Синтез та резорбція амніотичної рідини
У ранні терміни вагітності вся поверхня амніона виконує секреторну функцію. У пізніші терміни обмін відбувається переважно через амніотичну поверхню плаценти.
Крім того, навколоплідні води поповнюються за рахунок надходження в амніотичну порожнину сечі плода.
Повний обмін навколоплідних вод відбувається за 3 год.
Приблизно в 50 % випадків причину патології навколоплідних вод виявити не вдається. Баланс амніотичної рідини — процес автономний, тому не залежить від споживання рідини вагітною.
Однак дані Кокранівського керівництва (2010) свідчать про те, що гідратація вагітної збільшує об’єм амніотичної рідини і може сприяти усуненню маловоддя.
Походження амніотичної рідини в І триместрі:
транссудація материнської плазми через хоріон/амніон;
транссудація плазми плода через шкіру плода до початку її кератинізації.
У ІІ триместрі амніотична рідина є продуктом плодової сечі та легеневої рідини.
Резорбція забезпечується ковтанням рідини плодом і переходом її через плодові оболонки у материнський кровотік.
Наприкінці вагітності легені плода утворюють 300-
Напередодні пологів плід виробляє близько 400-
У кінці вагітності плід ковтає 200-
Деяка кількість амніотичної рідини проходить через оболонки до плодових плацентарних судин.
Об’єм амніотичної рідини досягає максимуму, збільшуючись до 800 мл у 36 тиж, зменшується до 500 мл близько 40-
Баланс амніотичної рідини підтримується шляхом
продукції сечі нирками плода,
утворення легеневого секрету,
резорбції навколоплідних вод при заковтуванні їх плодом,
обміну речовин між плодовими оболонками і плацентою.
Розлади будь-
УЗД — основний метод визначення об’єму амніотичної рідини.
Використовують індекс амніотичної рідини (ІАР).
ІАР вираховують у такий спосіб: живіт матері умовно поділяють на 4 квадранти, визначають величину вертикального стовпа амніотичної рідини в кожному квадранті, виражену в сантиметрах, і додають одержані значення.
-
-
Маловоддя
Маловоддям вважається об’єм амніотичної рідини менше 300—500 мл.
Частота
Частота розвитку маловоддя становить 0,7—5,5 %. Показник перинатальної смертності при цій патології — 17,7— 104,9 %о.
Між маловоддям і вродженими вадами розвитку (ВВР) плода існує чітка залежність: за його наявності цей показник сягає 54 %.
У 89 % випадків при маловодді спостерігається ЗРП. Вкрай несприятлива прогностична ознака — поєднання маловоддя із ЗРП, що виникає в II триместрі вагітності і призводить до її переривання, антенатальної загибелі плода або смерті новонародженого в перші дні життя.
При маловодді частота дистресу плода під час пологів становить 10 %, ризик інфікування плода зростає в 5 разів, ознаки інфікування новонароджених у 1,6 % , пневмонія — у 4,9 % випадків.
Причини
Маловоддя є наслідком втрати амніотичної рідини або зменшення секреції чи виділення плодом сечі.
Маловоддя пов’язане з однією із чотирьох причин:
розрив навколоплідних оболонок;
порушення роботи нирок, сечовидільної системи плода;
хронічне зменшення сечі внаслідок зменшення ниркової перфузії;
переношена вагітність (причина цього остаточно невідома).
Крім того, маловоддя може бути зумовлене:
патологією плода (затримка розвитку плода (ЗРП), внутрішньоутробні інфекції, хромосомні аномалії);
патологією плаценти (плацентарна дисфункція, аномалії розвитку, множинні інфаркти);
антенатальною загибеллю плода;
ідіопатичними чинниками (більше ніж у 50 % випадків причини залишаються нез’ясованими);
ятрогенними чинниками;
синдромом фето-
Класифікація
Маловоддя може бути гострим і хронічним, помірним і вираженим.
Діагностика
попередній діагноз встановлюють при зменшенні окружності живота, висоти дна матки до гестаціного віку (висоту стояння дна матки порівнюють із гравідогравою),
виявлення симптомів передчасного розриву плодових оболонок,
можливе зниження рухової активності плода,
під час пологів визначається плоский плодовий міхур,
підтвердження маловоддя обов'язкове на УЗД -
визначення точного гестаційного віку і стану плода (діагностика затримки внутрішньоутробного росту, переношеністі),
за показаннями виконують амніоцентез і каріотипування,
УЗД для виключення аномалій розвитку плода.
Лікування. Акушерська тактика при маловодді
До 22 тижнів
вирішити питання про доцільність продовження вагітності (високий перинатальний ризик у вагітних із ЗРП на тлі маловоддя, яке розвинулося в II триместрі).
Переривання вагітності за медичними показаннями на тлі патології навколоплідних вод проводять у разі:
поєднання маловоддя чи багатоводдя з внутрішньоутробною вадою розвитку (ВВР) плода;
гострого маловоддя, що розвинулося до 22 тиж. вагітності.
Після 22 тижня
комплексне обстеження для визначення стану плацентарного комплексу.
маловоддя в III триместрі + ЗРП → медикаментозна терапія ЗРП ефективна у 12,1 % жінок із маловоддям і у 57,3 % вагітних із нормальною кількістю навколоплідних вод.
маловоддя в III триместрі + немає порушень розвитку плода → доношування вагітності та народження здорової дитини.
вроджена аномалія розвитку → консультація генетика, і розродження обговорюється разом з неонатологами і дитячими хірургами.
глибока недоношеність + нез’ясована причина маловоддя → вичікувальна тактика.
розрив плодових оболонок + доношена вагітность + відсутня пологова діяльність → індукція пологів.
плід доношений або переношений → індукція пологів.
меконій в навколоплідних водах або децелерації ЧСС на КТГ → амніоінфузія.
Перебіг пологів на фоні маловоддя
ускладнення
слабкість пологової діяльності внаслідок плоского плодового міхура та порушення процесів ретракції і дистракції м’язових волокон шийки матки;
гіпоксія плода;
компресія пуповини й інтранатальна загибель плода;
неправильне положення плода;
післяпологові кровотечі.
Ведення пологів при маловодді
ранній розтин плодового міхура (на початку І періоду пологів або одразу після діагностування маловоддя);
своєчасне розродження шляхом операції кесаревого розтину за наявності показань.
Багатоводдя
Багатоводдям вважається об’єм амніотичної рідини більше 1500—2000 мл.
Частота
коливається від 0,13 до 3 %
мертвонародження при багатоводді -
збільшується кількість дітей із низькою масою тіла при народженні внаслідок загрози переривання вагітності та ЗРП.
У зв’язку зі збільшенням частоти акушерської патології в жінок із багатоводдям підвищується кількість оперативних втручань.
Класифікація
багатоводдя може бути гострим і хронічним, помірним і вираженим.
Етіологія
Вирішальна роль у розвитку багатоводдя належить плаценті та навколоплідним оболонкам.
Причини багатоводдя:
пов’язані із захворюванням матері (цукровий діабет, інфекційні та запальні процеси);
пов’язані з патологією плода (порушення процесу заковтування амніотичної рідини, нейром’язові порушення, обструкція травного тракту, хромосомні аномалії, пухлини обличчя та шиї, гемолітична хвороба новонароджених, неімунна водянка плода, внутрішньоутробні інфекції);
фето-
пов’язані з патологією плаценти (хоріонангіома, плацента, оточена валиком);
ідіопатичні (більше ніж у 60 % випадків причини багатоводдя невідомі).
Діагностика
значне випередження показників ВДМ і окружності живота у порівнянні з терміном вагітності,
пальпаторно матка напружена,
пальпаторно виявляють флюктуацію та підвищену рухливість плода,
погано вислуховується його серцебиття,
збільшення індексу амніотичної рідини (ІАР) > 25 см, або найбільшого вертикального стовпа > 8 см.
лабораторні дослідження
серологічне дослідження крові на резус-
обстеження на інфекції,
виявлення прихованого цукрового діабету
амніоцентез,
каріотипування.
Попередній діагноз багатоводдя можна встановити під час зовнішнього акушерського дослідження. Диференціювати багатоводдя слід від багатопліддя, крупного плода.
Особливості перебігу пологів при багатоводді
Під час пологів за наявності багатоводдя у 3,1 % випадків спостерігають такі ускладнення:
передчасне вилиття навколоплідних вод;
неправильне положення плода (поперечне, косе);
слабкість пологової діяльності внаслідок перерозтягування матки;
випадання петель пуповини або дрібних частин плода під час вилиття навколоплідних вод;
гіпотонічні й атонічні кровотечі в ранній післяпологовий період;
передчасне відшарування нормально розташованої плаценти.
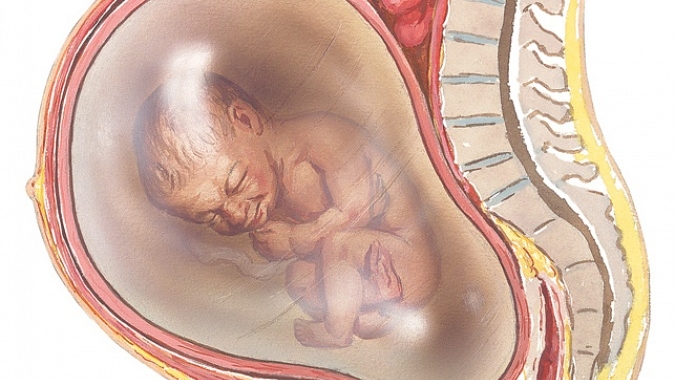
Мал. Багатоводдя одна з причин утворення тазового передлежання.
Особливості амніотомії на тлі багатоводдя
навколоплідні води слід випускати поступово;
для запобігання швидкому ви литтю амніотичної рідини амніотомію виконують у бічному сегменті вище внутрішнього вічка;
у разі розриву навколоплідних оболонок руку тримають у піхві для запобігання випаданню пуповини плода;
при пологостимуляції введення окситоцину починають через 2 год після вилиття навколоплідних вод для профілактики передчасного відшарування плаценти;
III період пологів ведуть на тлі застосування утеротонічних засобів.
Профілактика багатоводдя
виявлення в ЖК вагітних з групи високого ризику виникнення маловоддя або багатоводдя:
жінки з гіпертонічною хворобою,
цукровим діабетом,
хронічними інфекційними захворюваннями,
порушеннями обміну речовин,
резус-
ВВР плода в анамнезі,
багатоплідною вагітністю
своєчасна діагностика та лікування ускладнень вагітності,
активне виявлення латентних вогнищ урогенітальної інфекції та своєчасне лікування;
лікування цукрового діабету та артеріальної гіпертензії з ранніх термінів гестації;
застосування засобів, які покращують матково-
госпіталізація в стаціонар після встановлення діагнозу патології навколоплідних вод.
Прогноз вагітності залежить від етіології маловоддя чи багатоводдя. У 60 % випадків причину патології встановити не вдається.
Гестаційна трофобластична хвороба
Визначення
Гестаційна трофобластична хвороба (ГТХ) — різноманітна група взаємопов’язаних захворювань, які супроводжуються аномальною проліферацією трофобластної (плацентарної) тканини, внаслідок запліднення яйцеклітини сперматозоїдом з аномальним вмістом ДНК.
Ці пухлини здатні продукувати хоріонічний гонадотропін людини (ХГЛ), який використовується і як пухлинний маркер, і як скринінговий тест для контролю за ефективністю лікування.
Гестаційна трофобластична хвороба є винятково чутливою до хіміотерапії.
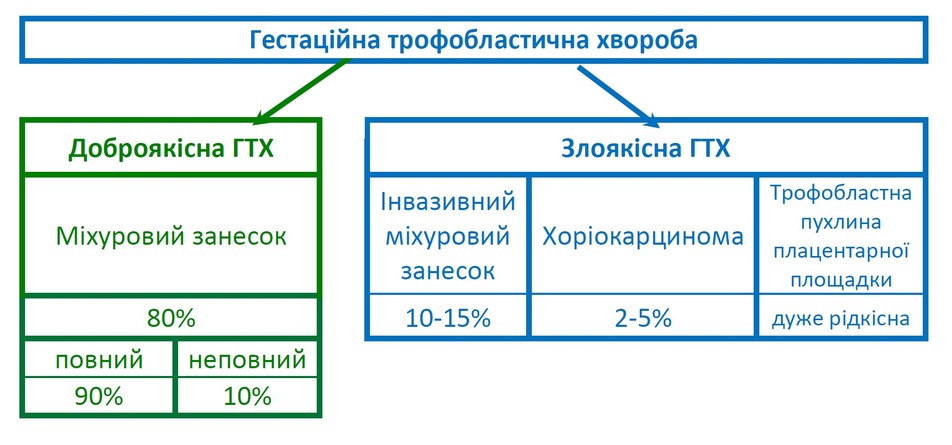
Класифікація
1. міхуровий занесок (молярна вагітність, 80 % випадків),
2. інвазивний міхуровий занесок (10–15 % ),
3. хоріокарцинома (2–5 %)
4. трофобластна пухлина плацентарної площадки (дуже рідкісна).
Класифікація гестаційної трофобластичної хвороби
Повний міхуровий занесок
Патогенез
Хоча причина цього захворювання залишається невідомою, вважають, що більшість випадків повного міхурового занеска виникають внаслідок фертилізації без’ядерної яйцеклітини («порожнього яйця»), в якій ядро втрачене або не функціонує, одним нормальним сперматозоїдом. Отже, всі хромосоми продукту запліднення в цьому разі мають батьківське походження.
В 90 % випадків повний міхуровий занесок має каріотип 46,ХХ, в 10 % випадків — 46,XY.
У рідкісних випадках повний міхуровий занесок утворюється при фертилізації порожньої яйцеклітини двома нормальними сперматозоїдами.
Частота
Частота міхурового занеска коливається від 1:200 до 1:1000 вагітностей у різних країнах світу, збільшуючись в азіаток.
Фактори ризику
Гестаційна трофобластична хвороба виникає у репродуктивному віці (20–40 років).
Зростання частоти захворювання має місце в тих географічних зонах, де дієта є бідною на бета-
Частіше ГТХ розвивається у жінок, які мали в анамнезі самовільні викидні або міхуровий занесок.
Клініка
скарги
нерегулярні або значні піхвові кровотечі в ранньому терміні вагітності (в 97 % випадків)
кровотеча неболюча, але може бути з матковими скороченнями
інші стани, подано в таблиці.
Об’єктивне обстеження
при гінекологічному дослідженні може спостерігатись
експульсія гроноподібних молярних часточок у піхву
кровотеча з цервікального каналу
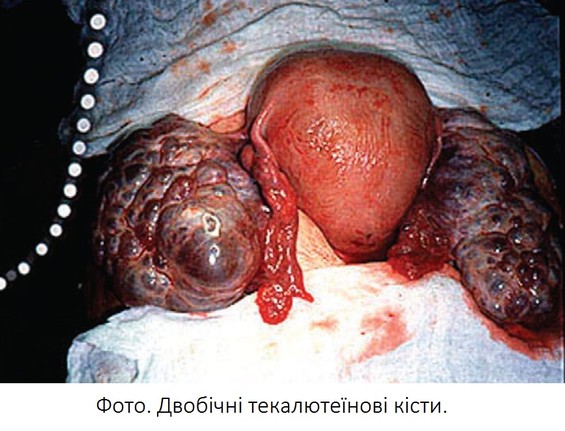
можуть бути виявлені двобічні тека-
невідповідність матки гестаційному віку
відсутність серцебиття і рухів плода
ознаки прееклампсії -

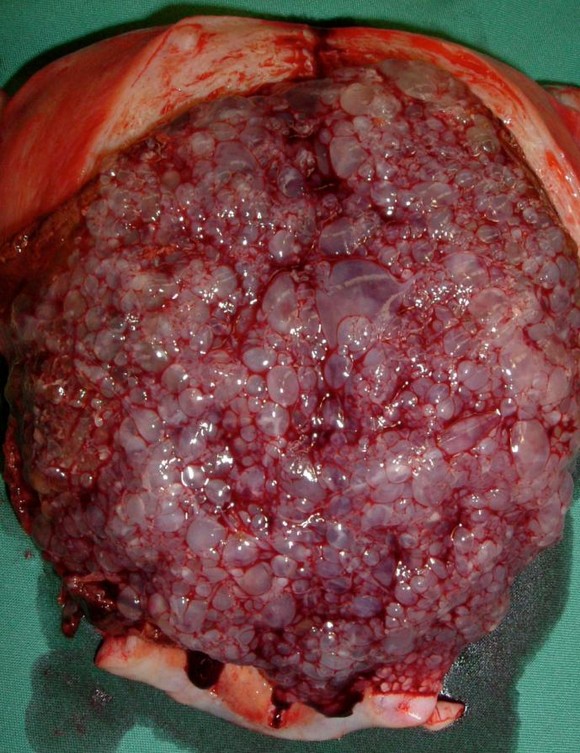
Фото. Мактопрепарат: порожнина видаленої матки повністю заповнена гроноподібними часточками міхурового занеска.
Діагностика
рівень ХГЛ є значно вищим (> 100 000 мМО/ мл), ніж при нормальній вагітності
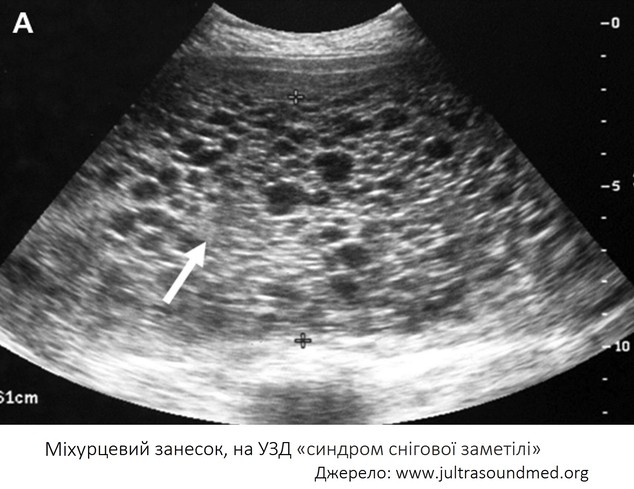
УЗД: «синдром снігової заметілі», у разі повного занеска елементи плода не візуалізуються.
Лікування
термінове видалення вмісту матки.
вакуум-
внутрішньовенне введення окситоцину
альтернативним варіантом лікування є гістеректомія.
Прогноз
Прогноз міхурового занеска є сприятливим (95–100 % випадків ефективного лікування).
Ризик рецидивного захворювання становить 3–5 %, навіть у разі гістеректомії.
Персистенція захворювання спостерігається у 15–25 % пацієнток із повним і у 4 % — з частковим занеском.
Ризик розвитку ГТХ при подальшій вагітності становить 1–5 %.
Моніторинг хворих
Контрольні дослідження рівня β-
Після цього щомісячний моніторинг рівня β-
Протягом періоду моніторингу пацієнтка повинна утримуватися від вагітності.
Пацієнтки після успішного лікування міхурового занеска не мають зростання ризику самовільних абортів і природжених аномалій розвитку.